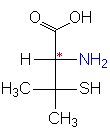
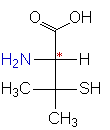
D-Penicillamin (D-2-Amino-3-mercapto-3-methyl-buttersäure) ist ein Abbauprodukt
des Penicillins und wird durch Hydrolyse aus diesem gewonnen. Bei der chemischen
Synthese fällt Penicillamin als Racemat an. Als Medikament darf nur hochreines
D-Penicillamin verwendet werden, da sein Enantiomer giftig ist.
D-Penicillamin kommt bei der
Wilsonschen Krankheit
(Morbus Wilson, hepatolentikuläre Degeneration) als Medikament zur
Kupfer-Ausscheidung zum Einsatz. Dabei wird die hohe Affinität der
Thiol-Gruppe zu Kupfer und die chelatbildende Eigenschaft des Moleküls
ausgenutzt. Aus dem gleichen Grund kann D-Penicillamin auch bei
Schwermetallvergiftungen mit Blei, Cadmium und Quecksilber gegeben werden.
Außerdem ist das Molekül durch seine Thiol-Aktivität in der
Lage, die Disulfid-Brücke von Cystin und Homocystin zu spalten und wird
daher zur Auflösung von Cystin-Harnsteinen eingesetzt.
Das L-Penicillamin ist dagegen hochgiftig.
Es besitzt die gleiche Konfiguration wie die proteinogenen Aminosäuren
und greift daher massiv in den Aminosäure-Stoffwechsel ein.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie