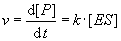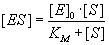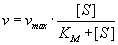Eine enzymkatalysierte Reaktion läßt sich vereinfacht durch folgende Reaktionsgleichung
beschreiben:
E + S  ES
® E + P
ES
® E + P
E = Enzym, S = Substrat, P = Produkt
Für die Reaktionsgeschwindigkeit v gilt dann:
Die Reaktionsgeschwindigkeit wird von der Konzentration des Enzym-Substrat-Komplexes
bestimmt. Ist die Substratkonzentration deutlich größer als die Enzymkonzentration,
hängt [ES] nur von der Enzymkonzentration ab, es handelt sich um eine Reaktion 0. Ordnung.
Ist der größte Teil des Substrates umgesetzt, können nicht mehr alle Enzymmoleküle
mit Substrat beladen werden, es wird auch der [S]-Einfluß sichtbar. Der Zusammenhang wird
durch die Michaelis-Menten-Gleichung beschrieben:
KM bezeichnet hierin die Michaelis-Konstante, [E]o
die Gesamt-Enzymkonzentration.
Bezogen auf die Reaktionsgeschwindigkeit v erhält man:
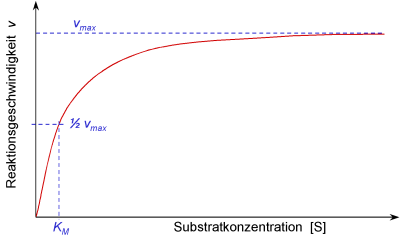
Trägt man die Reaktionsgeschwindigkeit gegen die Substratkonzentration auf, wird der
Zusammenhang nochmals verdeutlicht: Die maximale Reaktionsgeschwindigkeit wird nur bei
sehr hohen Substratkonzentrationen erreicht, denn dann sind alle Enzyme aktiv, d.h.
sie liegen als Enzym-Substrat-Komplex vor.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie
 ES
® E + P
ES
® E + P