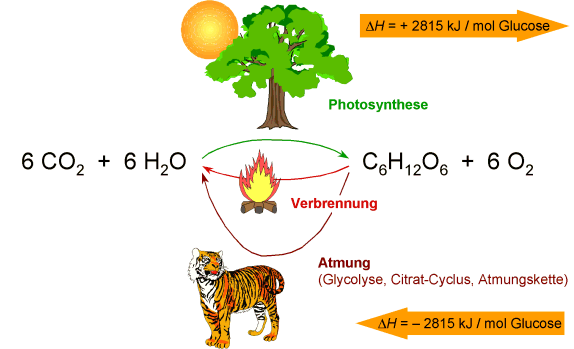
Der Satz von Heß kann auch auf biologische Vorgänge angewandt werden. Der Energieumsatz
bei der Bildung von Glucose aus Kohlendioxid und Wasser ist genau so groß wie der Umsatz
bei der Verbrennung von Glucose, nur das Vorzeichen ändert sich. Für den Energieumsatz
spielt es auch keine Rolle, ob die Verbrennung im Feuer durchgeführt wird oder über enzymatische
Prozesse in einem Lebewesen über viele Stufen abläuft.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Mar 30 11:42:03 2001 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie