 |
Natriumionen sind die wichtigsten Kationen des Extrazellularraumes (ca. 142 mmol/l). In der Zelle
herrschen dagegen Kaliumionen vor, die Natriumkonzentration beträgt intrazellulär nur
ca. 20 mmol/l. Dieses Konzentrationsgefälle wird durch aktiven Transport (d.h. unter ATP-Verbrauch)
aufrecht erhalten. Durch den Konzentrationsunterschied wird zwischen Cytoplasma und Extrazellularraum
ein Ruhepotential aufgebaut.
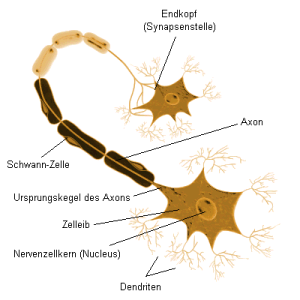
Bei der Reizleitung im Neuron wird durch Öffnen entsprechender Natrium- bzw. Kaliumkanäle
das Potential lokal kurzzeitig umgekehrt. Dieser elektrische Impuls wird dann weitergeleitet.
|
Der menschliche Organismus enthält etwa 140 g Kalium. 98% finden sich
intrazellulär und nur 2% im Extrazellularraum und im Blutplasma.
Schwankungen des K+-Spiegels wirken sich in hohem Maße
auf die Funktion der Zellen aus. Daher wird der Kaliumgehalt des Plasmas
in engen Grenzen gehalten. Kommt es zu einem Kaliumüberschuß
(Hyperkaliämie),
treten Parästhesien (Taubheitsgefühl) und Lähmungen auf,
von denen auch der Herzmuskel betroffen sein kann. Es kommt dann zu
Kammerflimmern oder Kammerstillstand: Herztod.
Ursache für einen Hyperkaliämie können Störungen der
Kaliumausscheidung (z.B. bei Niereninsuffizienz oder Nierenversagen),
Nekrosen größerer Zellverbände, Hämolyse oder
intravenöse Zufuhr von Lösungen mit höherer
Kaliumkonzentration sein. Letzteres kommt beispielsweise bei der
Transfusion älterer Blutkonserven vor, da die Erythrozyten
bei der Lagerung K+-Ionen freisetzen.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie
