| Elektrophile Substitution am Aromaten |
Das aromatische System des Benzols ist sehr stabil. Benzol reagiert daher ohne Katalysator
nicht mit Halogenen oder Oxidationsmitteln. Mit einem geeigneten Katalysator geht Benzol
mit Brom eine Reaktion ein. Dabei erfolgt aber - im Gegensatz zu den Alkenen - keine
Addition sondern eine Substitution.
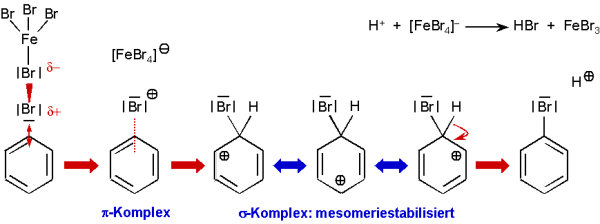
Das folgende Schema zeigt den Mechanismus dieser Substitutionsreaktion. Br2 bildet
mit dem Katalysator FeBr3 einen Komplex. Dieser kann sich an das p-System des
Benzols anlagern.
Nun erfolgt - analog zur Addition - eine heterolytische Spaltung der Br–Br-Bindung.
Der hierbei gebildete p-Komplex geht in einen s-Komplex über, bei dem das
Bromatom an einem C-Atom lokalisiert ist. Die positive Ladung ist über das mesomere
System delokalisiert. Nun wird ein Proton abgespalten, wobei das aromatische System wieder
zurückgebildet wird. Das abgespaltene Proton kann mit [FeBr4]–
zu HBr und dem Katalysator FeBr3 reagieren.
Da diese Reaktion durch einen Angriff am elektronenreichen p-System eingeleitet wird,
bezeichnet man diesen Reaktionstyp als elektrophile Substitution.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Feb 1 11:42:37 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
| 

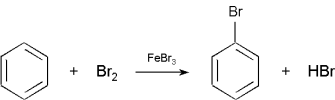
 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie