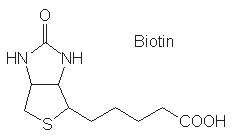
Biotin besitzt einen bicyclischen Bau, wobei es sich beim
(in der Abbildung) oberen Ring um ein Harnstoff-Derivat handelt. Biotin ist die
prosthetische Gruppe der Carboxy-Transferasen. Es ist über
die Carboxylgruppe mittels einer Peptid-Bindung an einen Lysinrest des Enzyms gebunden.
Biotin-Enzyme sind beispielsweise an der Gluconeogenese (Pyruvat-Carboxylase) und am
Fettsäurestoffwechsel (Propionyl-CoA-Carboxylase) beteiligt.
Biotin kommt in den meisten Nahrungsmitteln vor, besonders Biotin-reich
sind Leber und Eigelb. Außerdem wird das Vitamin von der Darmflora gebildet. Ein
Biotinmangel kann bei längerdauernder Zerstörung der Darmflora auftreten oder künstlich
erzeugt werden, wenn große Mengen rohen Eiklar gegessen werden (würden). Im rohen Eiklar
ist das Protein Avidin enthalten, das mit Biotin einen stabilen Komplex eingeht,
der auch von Proteasen nicht angegriffen werden kann. (Avidin wird beim Kochen
denaturiert, bei gekochten Eiern besteht diese Gefahr also nicht.)
Die Symptome des Biotinmangels sind unspezifisch: Dermatitis, Haarausfall,
neuronale Störungen.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie