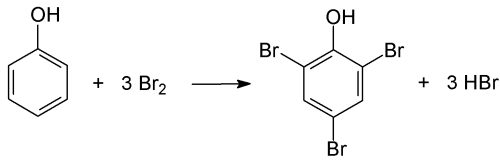
Durch die gebundene OH-Gruppe am aromatischen System sind die Positionen am Ring nicht
mehr äquivalent. Eine Zweitsubstitution erfolgt an Phenol ausschließlich in
ortho- oder para-Stellung. Werden drei Äquivalente Brom umgesetzt, entsteht 2,4,6-Tribrom-phenol.
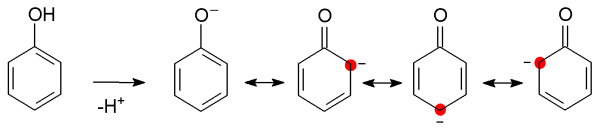
Die OH-Gruppe ist, vor allem durch die freien Elektronenpaare am Sauerstoff, am p-System
beteiligt und greift in das mesomere System ein. Die Grafik zeigt die möglichen mesomeren
Grenzstrukturen am Beispiel des Phenolat-Ions. Es wird deutlich, daß nur an den
C-Atomen in ortho- und para-Stellung eine höhere Elektronendichte vorliegt, da nur dort
eine negative Partialladung lokalisiert werden kann. Daher erfolgt auch nur an diesen
Stellen eine elektrophile Substitution.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie