Molekulare Oberflächen
Zweidimensionale Strukturdiagramme und 3D Molekülstrukturen
können die Basis bilden, um viele chemische und physikalische
Eigenschaften von Verbindungen zu beschreiben. Alle bisherigen Modelle
stellen maximal nur das 3D Skelett des Moleküls und nicht dessen
wirkliche räumliche Ausdehnung dar.
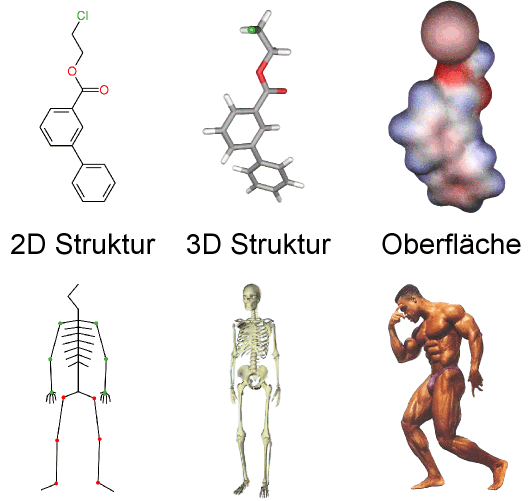
In Analogie zum menschlichen Körper, mit Skelett und den umgebenden
Organen und Geweben mit begrenzender Oberfläche (der Haut),
können Moleküle als Objekte mit Moleküloberfläche
angesehen werden. Die Oberfläche trennt den 3D Raum in einen
inneren Volumenteil, der vom Molekül ausgefüllt wird,
und einen äusseren Teil (den Rest des Universums). Dieses Bild
von einer exakten Trennung durch eine diskrete Oberfläche ist
allerdings nur eine Näherung,
da Moleküle nicht nach den gleichen Gesetzen der klassischen
Mechanik für makroskopische Objekte behandelt werden können.
Im quantenmechanischen Sinne besitzen Moleküle weder Körper
noch eine feste Oberfläche. Die Bestandteile eines Moleküls
sind Atome, die wiederum aus Protonen und Neutronen zusammengesetzt
sind, umgeben von Elektronen. Der Raum der von den Elektronen ausgefüllt
wird, ist nicht von einer Oberfläche eingeschlossen, sondern
ist durch eine "Elektronenwolke" charakterisiert. Die Elektronendichte
ist kontinuierlich und geht in großer Distanz zum Atomkern
gegen Null. Im Besonderen ist die Elektronenverteilung entscheidend
für die molekularen Wechselwirkungen, bestimmt aber auch die
Eigenschaften eines Moleküls. Üblicherweise werden aber
Atom- und Moleküloberflächen dadurch angegeben, daß
sie einen bestimmten Prozentsatz (z.B. 90%) der Elektronenverteilung
umschließen.
Moleküloberflächen können verschiedene Eigenschaften,
wie z.B. elektrostatisches Potential, Atomladung oder Hydrophobizität,
durch eingefärbte Kartierungen
(mapping) ausdrücken.
© Prof. Dr. J. Gasteiger, Dr. Th. Engel, CCC Univ. Erlangen, Thu Dec 18 14:53:54 2003 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie
