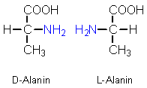Allgemeine Konzepte zur Isomerie organischer Verbindungen
Die Anordnung der Bindungen, die die Atome in einem Molekül untereinander verknüpft, bezeichnet die Topologie bzw. die Konstitution einer Verbindung. Ein Molekül kann aber mit einer bestimmten Summenformel mehrere unterschiedliche Strukturen aufweisen, was als Isomerie definiert ist. Isomere können in Konstitutionsisomere und Stereoisomere aufgeteilt werden.
Konstitutionsisomere sind Moleküle mit verschiedenen Konnektivitäten zwischen den Atomen. Die Strukturen können zum einen unterschiedliche funktionelle Gruppen besitzen (Strukturisomere) oder zum anderen die gleiche funktionelle Gruppe aber an unterschiedlichen Positionen (Positionsisomere).
Haben Verbindungen die gleiche Topologie (Konstitution) aber unterschiedliche Topographie (Geometrie) werden sie als Stereoisomere bezeichnet. Die Konfiguration drückt die unterschiedlichen Stellungen der Atome um ein Stereozentrum, Stereoachse, und Stereoebene im dreidimensionalen Raum aus, z.B. chirale Verbindungen (Enantiomere, Diastereomere, Atropisomere, Helicene, etc.) oder cis/trans (Z/E) Konfiguration. Können Stereoisomere durch eine Rotation um eine C-C Einfachbindung rotiert werden, bezeichnet man sie als Konformere.
Isomere
Die Verbindungen besitzen gleiche Summenformeln, unterscheiden sich jedoch in ihrem molekularen Aufbau. |
| Konstitutionsisomere |
Stereoisomere |
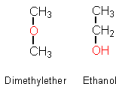
Strukturisomere
Bei Strukturisomeren sind unterschiedliche funktionelle Gruppen ausgebildet.
Beispiel: Ethanol - Dimethylether
 |
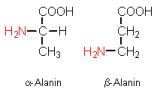
Stellungsisomere
Die gleichen funktionellen Gruppen sind an unterschiedliche Atome des Kohlenstoffgerüsts gebunden.
Beispiel: a-Alanin - b-Alanin
 |
Konfigurationsisomere
Die Isomere unterscheiden sich in der relativen Anordnung der Baugruppen zueinander. |
Konformationsisomere
Konformere können durch Rotation um C-C-Einfachbindungen ineinander umgewandelt werden.
Beispiel: n-Butan in der gauche- bzw. anti-Konformation
(Newman-Projektion)
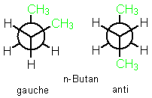 |
|
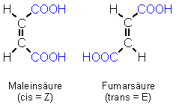
cis/trans- (Z/E-)
Isomere
Benachbarte Substituenten an Doppelbindungen oder Ringen können zwei verschiedene Anordnungen aufweisen.
Beispiel: Maleinsäure - Fumarsäure
Beispiel: 1,4-Cyclohexandiol
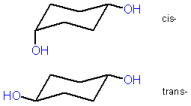
|
Enantiomere
Diastereomere
Besitzt das Molekül ein Chiralitätszentrum, ergeben sich zwei verschiedene Konfigurationen, die sich wie Bild und Spiegelbild verhalten (= Enantiomere). Sind mehrere Chiralitätszentren vorhanden, kommen noch Diastereomere dazu.
Beispiel: D-/L-Alanin (Enantiomere)
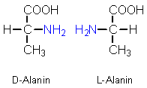 |
|
Axiale Chiralität (Atropisomerismus, Helicene)
Besitzt ein Molekül 4 Liganden, die paarweise um eine Achse plaziert sind und nicht in einer Ebene liegen, gibt es Atropisomere.
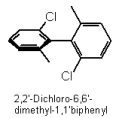
Ein Spezialfall axialer Chiralität ist die Anordnung des Moleküls als rechts oder links drehende Helix (Helicene).
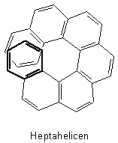
|
|
Planare Chiralität
Die Anordnung des Moleküls kann in unterschiedlichen Seiten differenziert werden.
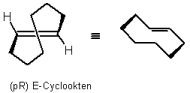
|
Eine einfache, aber detailliertere Einführung in die Isomerie organischer Verbindungen kann unter "Chemie für Mediziner" gefunden werden.
© Prof. Dr. J. Gasteiger, Dr. Th. Engel, CCC Univ. Erlangen, Thu Dec 18 14:53:54 2003 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie