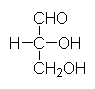
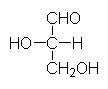
Triosen besitzen drei C-Atome. Bei den Aldotriosen ist das zweite C-Atom chiral.
Es gibt also zwei Enantiomere: D- und L-Glycerinaldehyd:
Es gibt auch eine Ketotriose: 1,3-Dihydroxyaceton. Dieser Zucker besitzt kein chirales
C-Atom. In der Glycolyse entstehen durch die Aldolase-Reaktion aus Fructose
je ein Molekül D-Glycerinaldehyd und Dihydroxaceton (in phosphorylierter Form).
Diese können durch eine Isomerase
ineinander umgewandelt werden. Es handelt sich hierbei um Tautomere,
d.h. bei der Isomerisierung werden nur H-Atomen umgelagert.
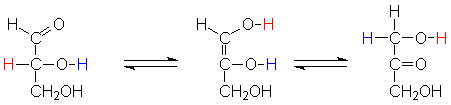
Keto-Enol-Tautomerie zwischen D-Glycerinaldehyd und Dihydroxyaceton |


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie