|
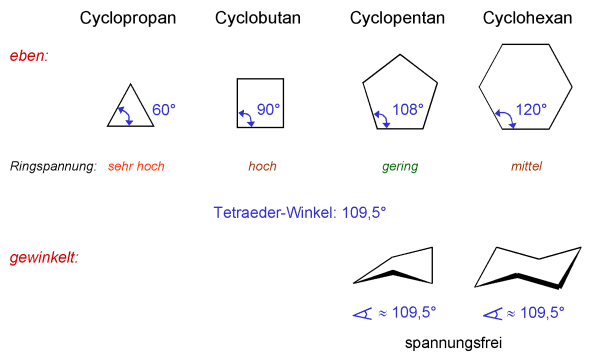
Die Moleküle der Cycloalkane werden oftmals als ebene Ringe gezeichnet.
Dies entspricht jedoch nicht der Realität. Wären die Cycloalkane eben gebaut,
besäßen sie sehr hohe Ringspannungen. Bei Cyclopropan, das zwangsläufig
(da aus drei Atomen bestehend) eben sein muß, ist dies auch der Fall: Die Bindungswinkel
betragen 60°, der spannungsfreie Tetraederwinkel, den die sp3-hybridisierten
Kohlenstoffatome anstreben, dagegen 109,5°. Auch Cyclobutan besitzt eine hohe Ringspannung.
Cyclopentan und Cyclohexan kann durch einen gewinkelten Bau der hohen Ringspannung ausweichen.
Zwar wäre bei einem eben gebauten Cyclopentan der Bindungswinkel mit 108° nahe dem
Tetraederwinkel, durch eine Faltung des Moleküls kann aber der ideale 109,5°-Winkel
erreicht werden. Das gleiche gilt für Cyclohexan. Planar mit 120° wäre die
Ringspannung relativ groß, durch den gewinkelten Bau wird aber auch hier ein
spannungsfreier Zustand mit 109,5°-Winkeln erreicht.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Feb 1 11:42:37 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie