|
Benzol besteht aus sechs sp2-hybridisierten Kohlenstoffatomen.
Auch hier bilden die mit je einem Elektron besetzten p-Orbitale ein ringförmiges
p-System aus.
Formal liegen in diesem Molekül alternierend angeordnet je drei Doppel- und
Einfachbindungen vor: die Doppelbindungen sind konjugiert.
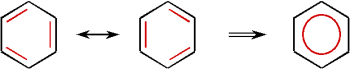
Bei diesem Molekül gibt es für die Lage der Doppelbindungen zwei äquivalente
Möglichkeiten. Tatsächlich sind alle C-C-Bindungen im Benzol gleichwertig.
Eine derartige Elektronenanordnung, bei der die Doppelbindungen "verschoben" werden
können, bezeichnet man als mesomer.
Oft wird dies durch die rechte Schreibweise angedeutet: Der Kreis soll anzeigen, dass es
keine isolierten Doppelbindungen gibt sondern ein geschlossenes p-System.
Geschlossene, ringförmige p-Systeme mit 4n+2 p-Elektronen nennt man
aromatisch. Zu den Aromaten gehören neben Benzol (mit 6 p-Elektronen) auch
Naphthalin (10 p-Elektronen) und Anthracen (14 p-Elektronen).
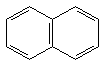
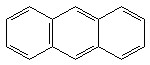 Naphthalin Anthracen
Naphthalin Anthracen
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Feb 1 11:42:37 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


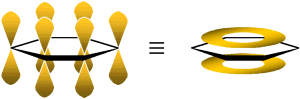


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie