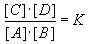Das Gleichgewicht kann auf die Seite der Produkte verschoben werden, wenn eines der Produkte
aus dem Reaktionsgemisch entfernt wird. Dies kann beispielsweise durch Abdestillieren oder
Ausfällen geschehen.
| A + B |
 |
C + D
Entfernung durch
Abdestillieren, Ausfällen etc. |
Da der Quotient der Konzentrationen der Produkte und der Edukte
konstant bleiben muß (= K), die Konzentration von C (durch
die Abdestillation, Ausfällung ...) aber verringert wird, verschiebt sich das
Gleichgewicht nach rechts. Die Konzentration von D nimmt zu und kompensiert
somit den Verlust an C.
Bei technischen Prozessen kann die Ausbeute einer Reaktion erhöht werden, indem
ein Produkt ständig aus dem Reaktionsgemisch entfernt wird. Auch in der Natur wird
dieses Prinzip ausgenutzt. Gleichgewichte werden auf die Seite der Produkte verschoben,
wenn die entstehenden Stoffe sofort weiterverarbeitet und damit aus dem Gleichgewicht
entfernt werden. Den Lebewesen ist es damit möglich, auch solche Reaktionen
zu nutzen, bei denen das Gleichgewicht eigentlich auf der Seite der Edukte liegt.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie