Darstellung chemischer Elemente
Die ersten Vorstellungen über Elemente und deren Aufbau entwickelten sich bereits im 5. Jahrhundert vor unserer Zeit. Feuer, Wasser, Erde und Luft wurden in der Vier-Elemente-Lehre formuliert. Damals wurden hauptsächlich die Metalle als reine Elemente (im heutigen Sinne) gewonnen, auch wenn sie noch nicht als solche erkannt wurden. Deren Bezeichnungen und Symbole (z.B. Planetensymbole) wurden bereits im Altertum niedergeschrieben; einige Beispiele sind hier aufgeführt:
Bis zum 17. Jhd. gab es keine eindeutigen Definition der chemischen
Grundbegriffe, wie Element, Verbindung und Mischung. Aber mit der
Entwicklung der Atomtheorie und der damit verbundenen besseren Vorstellung
über die Materie wurden auch solche Begrifflichkeiten geklärt.
Ab 1818 bezeichnete J.J Berzelius als erster systematisch chemische
Substanzen mit Hilfe der quantitativen Analyse und den durch R.
Boyle definierten Ausdruck "Element".
In den darauf folgenden Jahren wurden die Eigenschaften der Elemente näher erforscht, so daß bereits um 1800 erste Äquivalentgewichtstabellen erstellt wurden. Mit der Ausbildung der Atomtheorie wurden auch schnell die Zusammenhänge zwischen Atomgewicht und den Eigenschaften chemischer Elemente erkannt.
Bereits damals wurde versucht, Elemente mit ähnlichen Eigenschaften
in Gruppen zusammenzufassen. Um 1870 gelangen dann L. Meyer und
D.I. Mendelejew gleichzeitig (aber auf unterschiedlichem Wege) die
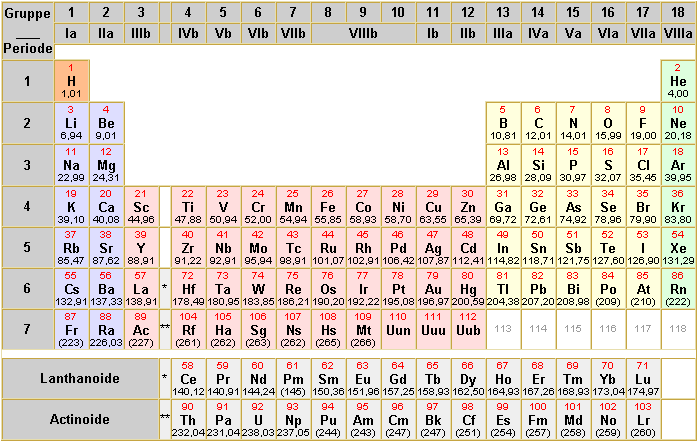
Zusammenstellung der Elemente zum Periodensystems der Elemente.
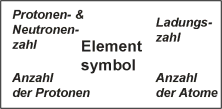
Heutige Nomenklatur:
Chemische Elemente werden in der Regel abgekürzt dargestellt. So hat jedes Element ein eigenes Symbol, das in der Regel aus dem großen Anfangsbuchstaben des wissenschaftlichen Namens und meist noch einem weiteren, klein geschriebenen charakteristischen Buchstaben besteht.
In der chemischen Zeichensprache kann am Element noch die Massenzahl, die Ordnungszahl, die Ionenladung und die Anzahl der Atome angegeben werden:
© Prof. Dr. J. Gasteiger, Dr. Th. Engel, CCC Univ. Erlangen, Thu Dec 18 14:53:53 2003 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|



 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie