|
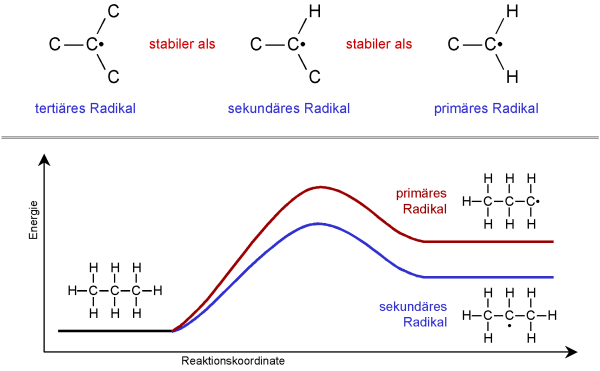
Je mehr Kohlenstoffatome an das C-Atom mit dem ungepaarten Elektron (also der Radikalfunktion)
gebunden sind, desto stabiler ist dieses Radikal. Ein tertiäres Radikal ist daher stabiler
als ein sekundäres und dieses wiederum stabiler als ein primäres Radikal.
Im Energiediagramm zeigt sich dieser Unterschied in der geringeren Energie des Radikals und der
reduzierten Aktivierungsenergie bei der Bildung.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Feb 1 11:42:37 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie