| Selektivität der Halogenierung |
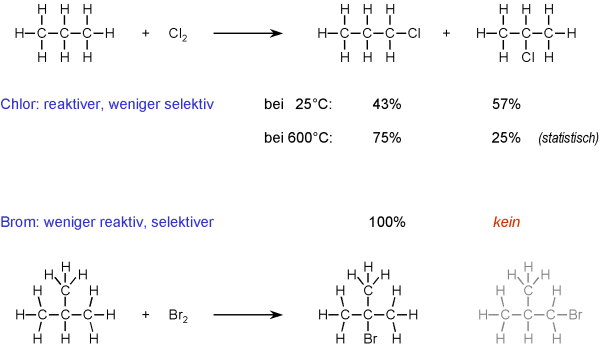
Bei den sehr reaktiven Halogenen Fluor und Chlor läuft die Halogenierungsreaktion sehr schnell ab.
Die unterschiedliche Stabilität der verschiedenen Radikale spielt nur eine geringe Rolle und hat
daher auch nur einen geringen Einfluß auf die Ausbeute der möglichen Produkte.
Bei der Chlorierung wirkt sich die Radikalstabilität nur bei niedrigen Temperaturen aus:
Das sekundäre Radikal wird etwa viermal so oft gebildet wird, als das primäre (bezogen auf
die abspaltbaren H-Atome). Bei hohen Temperaturen ist die Reaktion so schnell, daß kein
Einfluß der höheren Stabilität sekundärer Radikale mehr erkennbar ist:
Die Umsetzung erfolgt statistisch.
Brom zeigt dagegen eine deutlich geringere Reaktivität: Bei der Bromierung von Isobutan entsteht praktisch
ausschließlich 2-Brom-isobutan, das primäre Radikal (obwohl es statistisch 9mal so oft
gebildet werden kann) entsteht nicht.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Feb 1 11:42:37 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|



 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie