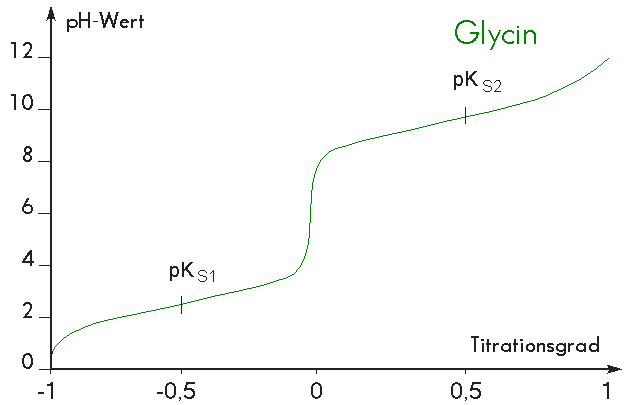
| Titrationskurve von Glycin |
Beim Titrationsgrad 0,5 zeigt die Aminosäure maximale Pufferwirkung. Das
Gleichgewicht zwischen Kationen und Zwitterionen bzw. Zwitterionen und Anionen liegt
"in der Mitte", d.h. bei Titrationsgrad -0,5: [K] = [Z] und bei 0,5: [Z] = [A].
Setzt man dies in die Henderson-Hasselbalch-Gleichung ein, erhält man: pH = pKS1
+ log [Z]/[K] = pKS1 + log 1 und da log 1 = 0 ergibt sich an diesen Stellen pH = pKS. Beim Titrationsgrad 0,5 kann man also in der
Titrationskurve die pKS-Werte ablesen.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Thu Oct 12 17:05:26 2000 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie