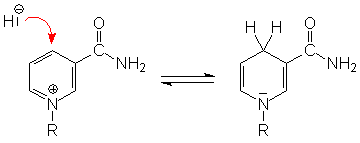| Zwei Vitamine und die daraus gebildeten Coenzyme sind Derivate des Pyridins:
Nicotinsäureamid und Pyridoxol besitzen einen Pyridinring.
Nicotinsäureamid ist, in Form der Coenzyme NAD/NADH und NADP/NADPH,
ein wichtiges Redox-System. Pyridoxalphosphat ist bei den meisten Prozessen
im Aminosäurestoffwechsel beteiligt. |
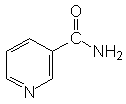
Nicotinsäureamid |
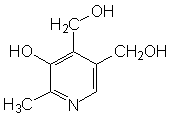
Pyridoxol |
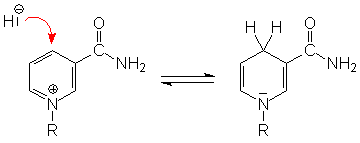
Die Redoxsysteme NAD+/NADH & NADP+/NADPH |
In den Coenzymen NAD+ und NADP+ ist ein
Molekül Nicotinsäureamid über eine
Pyrophosphatbrücke mit einem Adenosinrest verknüpft (R).
Die eigentliche Redox-Reaktion findet nur am Pyridin-Ring statt.
Aufgrund der quartären Ammonium-Gruppe ist das Ringsystem noch
elektronenärmer als das von Pyridin. Dies führt dazu,
daß an das Coenzym Nucleophile angreifen können.
Formal kann ein Hydrid-Ion angelagert werden, wobei der Stickstoff
und das para-ständige Kohlenstoffatom reduziert und das aromatische
System aufgehoben werden. In der Natur treten keine freien Hydrid-Ionen auf,
die Redox-Reaktion ist eingebunden in kompliziertere Reaktionsmechanismen.
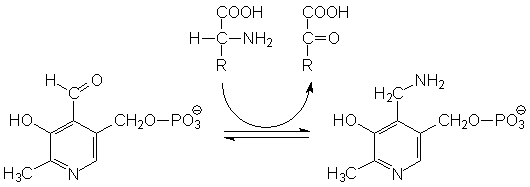
Transaminierung mit Pyridoxalphosphat |
Bei dem Coenzym Pyridoxalphosphat finden die Reaktionen nicht direkt am Ring statt.
Die Aminosäure wird an die Aldehydgruppe (unter Ausbildung einer
Schiffschen Base)
gebunden. Nun können verschiedene Reaktionen ablaufen. Hier wird der erste
Schritt einer Transaminierung gezeigt.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie