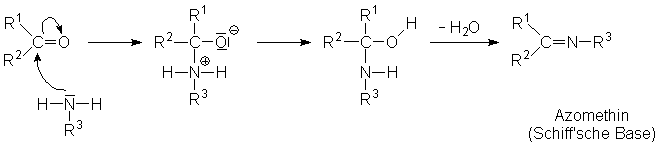
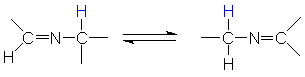Auch Ammoniak und Amine können Carbonylverbindungen als Nucleophile
angreifen. Das primäre Produkt der Addition stabilisiert sich, indem
ein Proton vom Stickstoff- auf das Sauerstoffatom übertragen wird. Das
tetraedrisches Zwischenprodukt ist jedoch nicht stabil und eliminiert Wasser
(Kondensation). Das endgültige Produkt ist ein Azomethin auch Schiff'sche
Base genannt.
Azomethine können z.T. auch tautomere Gleichgewichte ausbilden. Analog
zur Keto-Enol-Tautomerie wird dabei formal auch eine Doppelbindung um ein
Atom verschoben und ein H-Atom um zwei Atome verschoben.
Die Bildung Schiff'scher Basen ist eine sehr wichtige Reaktion im enzymatischen
Auf- und Abbau von Aminosäuren. Dabei reagiert die Aminogruppe der Aminosäure
mit der Carbonylgruppe von Enzymen zu einem Azomethin.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie