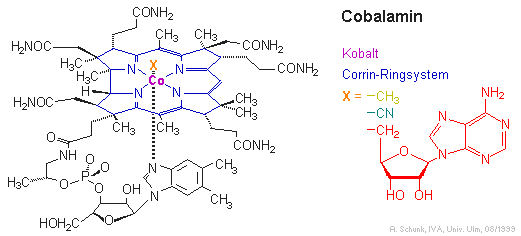
Das Zentrum der Cobalamine bildet ein oktaedrischer Kobalt-Komplex. Als Chelat-Ligand tritt hier ein
Corrin-System auf, das wiederum den Porphyrinen ähnelt. An das Corrin-System ist ein Pseudo-Nukleotid
gebunden, das eine axiale Position des Komplexes besetzt. Die sechste Koordinationsstelle kann beispielsweise
von einer Methylgruppe, einem Cyanidion oder einem Adenosylrest eingenommen werden. Aber auch andere
Liganden kommen vor.
Cobalamine spielen bei vielen katabolen Reaktionen eine wichtige Rolle, beispielsweise bei Methylierungen
und bestimmten Isomerisierungen.
Cobalamin kann vom Organismus nicht synthetisiert werden, es muß mit der Nahrung als
Vitamin B12 zugeführt
werden. Bei länger andauerndem Cobalamin-Mangel tritt die perniziöse
Anämie auf.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie