Cytochrome sind wichtige Redoxsysteme im Organismus. Sie kommen bei allen Lebewesen in sehr
ähnlichen Formen vor. Bei den Cytochromen handelt es sich um Proteine, in denen eine
Häm-Gruppe eingelagert ist.
Häm besteht aus einem Eisenion, das von einem vierzähnigen ringförmigen
Chelat-Liganden, dem Porphyrin, komplexiert wird. Da Eisen die Koordinationszahl 6 bevorzugt,
werden die zwei offenen Koordinationsstellen durch Aminosäure-Seitengruppen aus dem Protein
besetzt.
Das Eisenion in einem Cytochrom kann die Oxidationsstufen +2 und +3 annehmen. Cytochrome können
an Redox-Reaktionen teilnehmen, ohne zerstört zu werden. In der Atmungskette sind neben
dem freien Cytochrom c auch mehrere Cytochrome b in den verschiedenen Enzymkomplexen beteiligt.
Cytochrom P-450 ist eine Oxygenase, d.h. sie katalysiert die Oxidation organischer
Verbindungen durch Sauerstoff. Cytochrom P-450 kommt in vielen verschiedenen Formen vor (Isoenzyme) und ist
unter anderem an der Hydroxylierung von Steroiden und dem Abbau vieler Pharmazeutika und
Gifte beteiligt. |
|
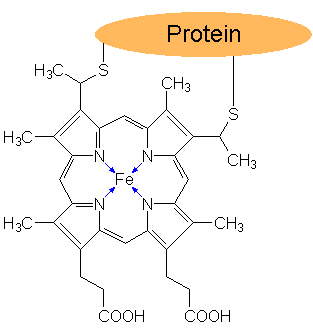
Häm A-Gruppe im Cytochrom c |


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie
