In den Molekülen eines Großteils der Naturstoffe liegen chirale
Kohlenstoffatome, also solche mit vier verschiedenen Substituenten, vor.
Man bezeichnet diese Kohlenstoffatome auch als Chrialitätszentren
und markiert sie im Molekül mit einem Stern.
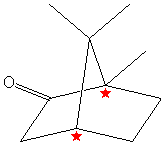
(+)-Campher |
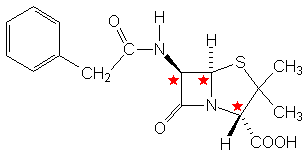
Penicillin G |
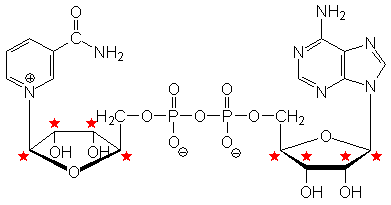
NAD+ |
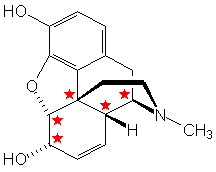
(-)-Morphin |
Die Abbildungen zeigen eine Auswahl chiraler Biomoleküle.
NAD+ enthält zwei Ribose-Moleküle mit jeweils vier
Chiralitätszentren. NAD+/NADH+H+ stellt ein
Redox-System dar, das als Coenzym von allen Lebewesen benötigt wird.
Penicillin G ist ein Antibiotikum, das von bestimmten Pilzen produziert wird.
Es leitet sich von Aminosäuren ab und enthält insgesamt drei chirale C-Atome.
Campher ist ein Terpen von stark aromatischem Geruch, Morphin ein Alkaloid.
Campher und Morphin sind nur in bestimmten Pflanzen enthalten.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie



