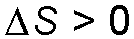Die Entropie des gesamten Systems bleibt bei völlig reversiblen Prozessen konstant,
bei irreversiblen Prozessen nimmt sie zu. Die Simulation zeigt schematisch zwei irreversible
Vorgänge, die von der Entropiezunahme angetrieben werden:
1. Wärmeaustausch zwischen zwei Körpern, bis diese die gleiche Temperatur besitzen;
2. Diffusion = Konzentrationsausgleich zwischen Lösungen.
© Prof. Dr. J. Gasteiger, Dr. A. Schunk, CCC Univ. Erlangen, Fri Mar 30 11:42:04 2001 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie