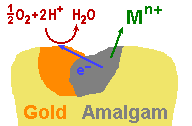In der Zahnheilkunde werden seit Jahrhunderten Amalgame (Legierungen von Quecksilber mit anderen Metallen)
als Füllmasse verwendet. Heute sind Legierungen gebräuchlich, die neben Quecksilber Silber,
Kupfer und Zinn enthalten. Unmittelbar nach Legen der Füllung beginnt die Oxidation durch
Luftsauerstoff. Dabei wird fast ausschließlich das unedelste Element, also Zinn, oxidiert.
Es bildet sich auf der Füllung eine Zinnoxid-Schicht, die nach einigen Tagen die Füllung
vollständig isoliert. Zu Beginn werden auch sehr kleine Mengen Quecksilber frei, nach 2 - 3
Wochen ist jedoch keine Quecksilber-Freisetzung mehr nachweisbar.
Wird nun jedoch in Nachbarschaft der Amalgam-Füllung ein edleres Metall eingebracht,
beispielsweise Gold, kann sich ein Lokalelement ausbilden. Voraussetzung ist, daß eine
elektrisch leitende Verbindung zwischen beiden Materialien vorliegt. Dies kann durch direkten Kontakt
oder über Zahnbein und Kiefer geschehen.
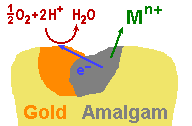 |
| Metalle im Amalgam: Sn, Cu, Ag, Hg |
| |
Sn2+ + 2 e– |
 |
Sn |
E° = –0,14 V |
| |
Hg2+ + 2 e– |
 |
Hg |
E° = +0,85 V |
| Sauerstoff: |
O2 + 2 H2O + 2 e– |
 |
4 OH– |
E° = +1,24 V |
| Gold: |
Au3+ + 3 e– |
 |
Au |
E° = +1,50 V |
|
Bei der Ausbildung des Lokalelementes erfolgt eine stark beschleunigte Korrosion der unedleren Metalle.
Insbesondere Zinn wird verstärkt oxidiert und die Elektronen werden an das Gold weitergeleitet.
An der Goldoberfläche nehmen Sauerstoffmoleküle die Elektronen auf und werden reduziert.
Bei diesem Gesamtprozeß werden neben Zinn auch kleine Mengen der anderen Amalgam-Metalle
oxidiert, also auch Kupfer, Silber und Quecksilber. Die entstandenen Ionen lösen sich im
Speichel und können im Verdauungstrakt resorbiert werden. Gesundheitliche Beeinträchtigungen
durch Quecksilberionen sind in diesem Fall nicht auszuschließen.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie