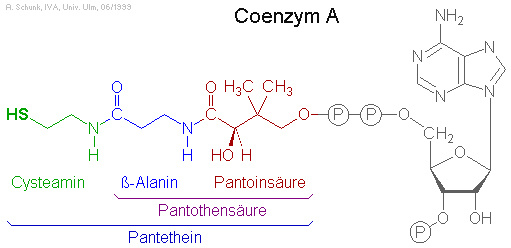
Coenzym A und Acyl-Carrier-Proteine enthalten zwei
biogene Amine: Cysteamin und b-Alanin. Acyl-Carrier-Proteine sind zentraler Bestandteil des
Fettsäure-Synthetase-Komplexes. Coenzym A erfüllt im katabolen und anabolen Stoffwechsel
wichtige Funktionen, insbesondere bei der Aktivierung, Umwandlung und Übertragung von
Acylgruppen. Die Carbonsäure-Derivate werden dabei an die HS-Gruppe des Cysteamin-Restes
gebunden. Man bezeichnet die CoA-Thioester daher als "aktivierte"
Säure-Derivate, beispielsweise Acetyl-Coenzym A (CoA-S~CO-CH3) als
"aktivierte Essigsäure".
Coenzym A und Acyl-Carrier-Protein besitzen einen Cysteamin-Rest, daran gebunden die
Pantothensäure (bestehend aus b-Alanin und Pantoinsäure).
Über zwei Phosphatreste ist diese Gruppe an einen Adenosin-Rest (bei Coenzym A) bzw.
über einen Phosphat-Rest an ein Serin der Carrier-Protein-Kette gebunden.


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie