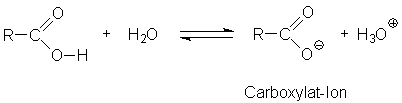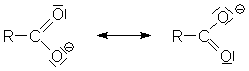Die niederen Carbonsäuren (ungefähr bis C4) sind bei
Raumtemperatur flüssig und vollständig mit Wasser mischbar. In wässriger
Lösung stellt sich folgendes Dissoziationsgleichgewicht ein.
Carbonsäuren gehören zu den organischen Verbindungen mit der stärksten
Tendenz Protonen abzugeben. Allgemein hängt die Acidität einer organischen
Verbindung R–H von folgenden Faktoren ab:
- Von der Elektronegativität des Atoms an welches, das H-Atom gebunden
ist. Ethan hat z.B. einen pKs-Wert im Bereich von 60, während
Ethanol einen pKs von » 16
aufweist.
- Von der Möglichkeit die negative Ladung des Anions R–
zu stabilisieren. Der pKs-Wert von Essigsäure liegt bei
4,8, während die Werte von Acetaldehyd, Ethanol und Aceton alle grösser
als 15 sind. Der Grund für die hohe Acidität der Essigsäure
liegt in der Stabilisierung der negativen Ladung im Carboxylat-Ion (Mesomerie).
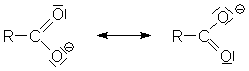
|
| Mesomerie des Carboxylat-Ions |
© Prof. Dr. J. Gasteiger, S. Spycher, CCC Univ. Erlangen, Thu Apr 25 13:32:19 2002 GMT
 BMBF-Leitprojekt Vernetztes Studium - Chemie BMBF-Leitprojekt Vernetztes Studium - Chemie
|


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie