Für viele Verbindungen sind auch heute die Trivialnamen am gebräuchlichsten.
| Name |
Anion |
Formel |
Kettenlänge |
| Ameisenäure |
Formiat |
H–COOH |
C1 |
| Essigsäure |
Acetat |
H3C–COOH |
C2 |
| Propionsäure |
Propionat |
H3C–CH2–COOH |
C3 |
| Buttersäure |
Butyrat |
H3C–(CH2)2–COOH |
C4 |
| Palmitinsäure |
Palmitat |
H3C–(CH2)14–COOH |
C16 |
| Stearinsäure |
Stearat |
H3C–(CH2)16–COOH |
C18 |
| Oxalsäure |
Oxalat |
HOOC–COOH |
C2 |
| Malonsäure |
Malonat |
HOOC–CH2–COOH |
C3 |
| Bernsteinsäure |
Succinat |
HOOC–CH2–CH2–COOH |
C4 |
Nach der Anzahl Carboxygruppen werden Mono-, Di- und Tricarbonsäuren unterschieden. Die letzten drei Verbindungen der Tabelle sind Beispiele für Dicarbonsäuren. Palmitin- und Stearinsäuren gehören zu den
den mengenmäßig bedeutendsten Verbindungen pflanzlicher und tierischer
Fette.
Die systematischen Namen setzen sich aus dem Namen des entsprechenden Kohlenwasserstoffs
und der Endung -säure zusammen. Das C-Atom der Carboxygruppe wird dabei
mitgezählt, z.B. Ethansäure für Essigsäure oder Butandisäure
für Bernsteinsäure.
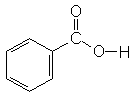
Die einfachste aromatische Carbonsäure heißt Benzoesäure.
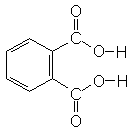
Phthalsäure ist eine aromatische Dicarbonsäure.
 |
 |
| Benzoesäure |
Phthalsäure |


 BMBF-Leitprojekt Vernetztes Studium - Chemie
BMBF-Leitprojekt Vernetztes Studium - Chemie

